Projekty
- Syntéza ligandů pro lektinový receptor DC-SIGN
- Syntéza agonistů muskarinových receptorů
- Syntéza ligandů pro vizualizaci G-kvadruplexů
Syntéza ligandů pro lektinový receptor DC-SIGN
DC-SIGN je lektinový receptor typu C, který se nachází na povrchu imunitních buněk, zejména dendritických buněk a makrofágů. Přirozenými ligandy DC-SIGN receptoru jsou oligo- a polysacharidy s vysokým obsahem manosy a fukosy.
Jednou z hlavních funkcí DC-SIGN receptoru je rozpoznávání sacharidů nacházejících se na povrchu řady patogenů: virů (např. HIV, Ebola, SARS-CoV-2), bakterií (M. tuberculosis, S. pneumoniae), hub (C. albicans) i parazitů (Leishmana). Po navázání patogenu dochází k jeho internalizaci do dendritické buňky a ke spuštění imunitní odpovědi. Některé patogeny (např. virus HIV) však interakci s DC-SIGN receptorem zneužívají ke svému šíření se po hostitelském organismu.
Kromě toho může DC-SIGN vysílat modulační signály, které buď stimulují, nebo tlumí imunitní odpověď v závislosti na typu navázaného ligandu. Podílí se také na buněčné adhezi.
Ligandy vážící se selektivně k DC-SIGN receptoru by mohly mít několikero praktické využití v medicíně:
1) Cílený transport léčiv (drug targeting) k dendritickým buňkám: ligandy interagující selektivně s DC-SIGN receptorem mohou být využity k cílenému doručování siRNA, antigenů nebo imunomodulátorů pomocí liposomů, dendrimerů nebo nanočástic.
2) Imunoterapie: Zacílení na dendritické buňky může pomoct zvýšit protinádorovou imunitu. Nanočástice modifikované určitým antigenem by mohly být využity k „tréninku“ dendritických buněk, aby daný antigen rozpoznaly.
3) Antimikrobiální látky: Selektivní inhibice receptoru DC-SIGN by nám mohla poskytnout možnost ovlivnit imunitní odpověď již v raných stádiích infekce a otevřít cestu k nové třídě léčiv pro terapii těchto onemocnění.
Sacharidové vazebné místo DC-SIGN receptoru je značně mělké a hydrofilní, a proto není jeho cílení v medicinální chemii příliš perspektivní. Nedávné studie prokázaly, že DC-SIGN receptor má kromě primárního sacharidového vazebného místa i několik sekundárních vazebných míst, která jsou k dispozici pro vazbu malých organických molekul (Obrázek 1).
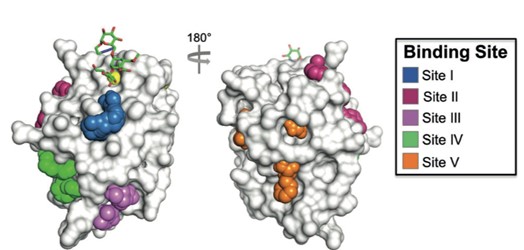
Obrázek 1. DC-SIGN receptor, primární sacharidové vazebné místo (žlutě) a sekundární vazebná místa I–V. Obrázek převzat z Aretz, J. et al.: Angew. Chem. Int. Ed. 2017, 56, 7292–7296.
Naším hlavním cílem je syntéza nových ligandů DC-SIGN receptoru, které se budou vyznačovat vysokou selektivitou a vhodnými vlastnostmi (drug-like properties). Připravujeme několik typů ligandů:
* Sacharidová glykomimetika – látky na bázi D-manosy nebo L-fucosy, nesoucí substituenty interagující buď s okolím sacharidového vazebného místa, nebo se sekundárním vazebným místem (Obrázek 2a).
* Allosterické ligandy – látky nesacharidového charakteru, které interagují se sekundárními vazebnými místy a svou vazbou k těmto místům ovlivňují vazbu sacharidů k primárnímu sacharidovému vazebnému místu (Obrázek 2b). K syntéze těchto látek využíváme fragmentový přístup, tzv. fragment-based drug discovery.
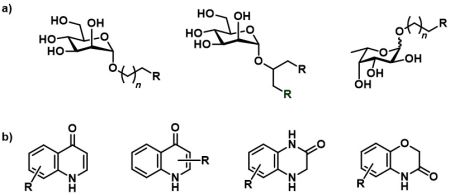
Obrázek 2. Příklady syntetizovaných ligandů pro DC-SIGN receptor. a) Ligandy DC-SIGN receptoru založené na D-manose a L-fukose; b) nesacharidové ligandy vážící se k sekundárním vazebným místům.
Na projektu spolupracujeme se skupinou prof. Christopha Rademachera z Univerzity ve Vídni. V jeho laboratoři probíhá testování afinity látek a formulace nanočástic pro cílený transport.
Syntéza agonistů muskarinových receptorů
Muskarinové acetylcholinové receptory jsou receptory spřažené s G proteinem, které jsou důležitou součástí mnoha signalizačních drah v lidském těle. Pět známých typů muskarinových receptorů (M1–M5) je hojně exprimováno jak v centrálním, tak v periferním nervovém systému. Každý z nich se může v různých tkáních podílet na udržování správného chodu několika různých fyziologických funkcí. Dosažení selektivity pro specifický podtyp receptoru a signální dráhu má zásadní význam pro vývoj léčiv cílených na muskarinové receptory, aby se minimalizovaly potenciální vedlejší účinky.
V roce 2020 byl výzkumnou skupinou Dr. Jakubíka objeven ligand na bázi tetrahydropyridinia (Obrázek 3a, slouží jako lead structure pro náš projekt), který vykazuje selektivitu pro muskarinové receptory M2 a tzv. signalizační bias směrem k Gi/o dráze napříč všemi podtypy muskarinových receptorů.
V rámci projektu se zabýváme syntézou agonistů muskarinových receptorů na bázi tetrahydropyridinu, které mají potenciál v léčbě neuropatické bolesti. Syntetická část projektu má tři hlavní cíle:
* Syntéza analogů naší lead compound pro studium vztahů mezi strukturou a aktivitou (SAR)
* Syntéza bitopických ligandů nesoucích jak ortosterický ligand (lead structure), tak allosterický ligand zvyšující afinitu k receptoru (Obrázek 3b)
* Syntéza nových typů ligandů předpovězených pomocí počítačového modelování
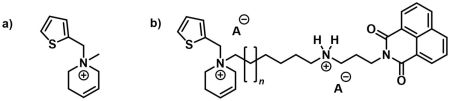
Obrázek 3. Příklady syntetizovaných ligandů pro muskarinové receptory. a) Vůdčí struktura (lead structure), b) příklad bitopického ligandu.
Na projektu spolupracujeme se skupinou dr. Jana Jakubíka z Fyziologického ústavu AV ČR. V jeho laboratoři probíhá testování afinity a selektivity látek.
Syntéza ligandů pro vizualizaci G-kvadruplexů
V rámci projektu se zabýváme syntézou ligandů pro vizualizaci G-kvadruplexů. Naším cílem je syntetizovat „dvojitě chytré“ fluorescenční sondy, které fungují jednak jako „chytrý“ ligand G-kvadruplexu (tj. vytvoří se pouze v přítomnosti přirozeného G-kvadruplexu) a jednak jako „chytrá“ fluorescenční sonda (tj. je fluorescenční pouze v přítomnosti svého cíle, tedy G-kvadruplexu). První látka z této série (N-TASQ), připravená spolupracující skupinou, byla použita k vůbec prvnímu zobrazení G-kvadruplexů v živých lidských buňkách (Obrázek 4), a od té doby byla využita v onkologii a neurologii. Naším cílem je připravit látky příbuzné N-TASQ a pokusit se vylepšit jeho vlastnosti.
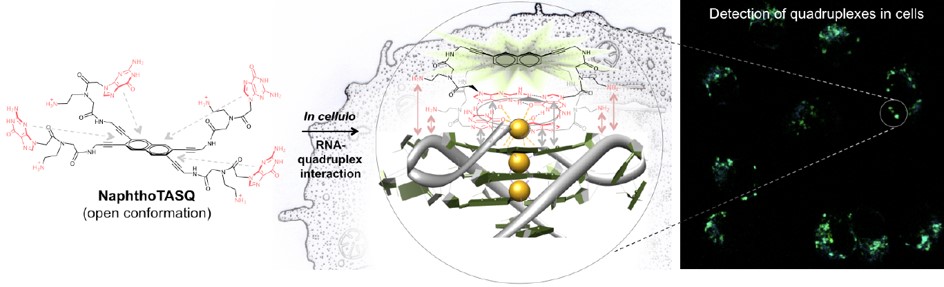
Obrázek 4. Dvojitě chytré sondy pro vizualizaci G-kvadrulpexu. Převzato z Laguerre, A. et al.: J. Am. Chem. Soc. 2015, 137, 8521–8525.
Na projektu spolupracujeme se skupinou dr. Davida Monchauda z ICMUB CNRS ve francouzském Dijonu. V jeho laboratoři probíhá studium připravených látek pomocí biofyzikálních metod.
